※本稿は、田中道昭『モデルナはなぜ3日でワクチンをつくれたのか』(インターナショナル新書)の一部を再編集したものです。
SARSで20カ月かかった時間を90%削減した
新型コロナウイルスの遺伝子情報が中国の科学者らによってインターネット掲示板に公開されたのが2020年1月10日でした。モデルナは、この遺伝子情報の開示を受けて、1月13日までに新型コロナウイルス・ワクチン候補の設計を完了、2月7日までにその臨床試験用ワクチンを製造し品質試験を実施、そして2月24日には臨床試験に向けてNIH(米国国立衛生研究所)へ送付したといいます。
遺伝子情報の開示からワクチン候補の設計完了まで、わずか3日。そしてワクチン候補の設計完了から臨床試験準備完了までの期間は、わずか42日。この42日は、これまで同じプロセスで最速であったのがSARSの時の20カ月ということですから、臨床試験の前工程にかかる時間が約90パーセント削減されたことになります。
続いて、NIH主導で3月16日にはフェーズⅠ臨床試験、5月29日にはフェーズⅡ臨床試験が開始され、7月27日にはNIHとBARDA(米国生物医学先端研究開発局)との共同でフェーズⅢ臨床試験が始まりました。10月22日には、米国の18歳以上の約3万人を対象とした臨床試験が終了。その後12月18日にモデルナの新型コロナウイルス・ワクチン「mRNA-1273」はFDA(米国食品医薬品局)によってEUA(緊急使用許可)が出され、すでに広く使用されるに至っています。
臨床試験完了までわずか9カ月というスピード
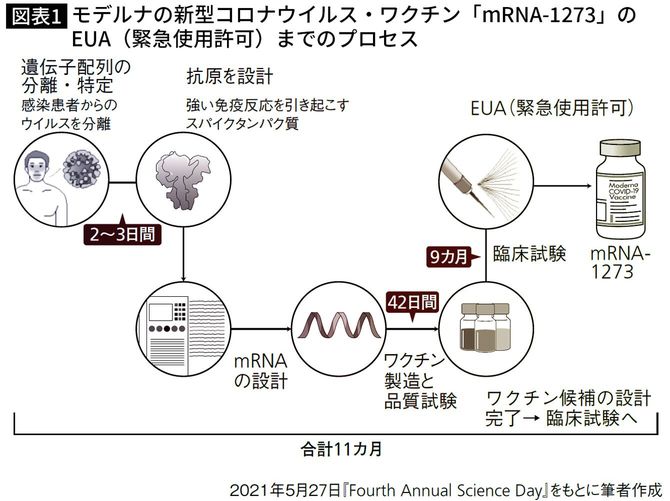
通常、ワクチンや薬の開発には、研究開発や実験、前臨床、フェーズⅠ~Ⅲの臨床試験、認可申請、審査も含めて10~15年程度かかると言われています。それが、モデルナは、新型コロナウイルスの遺伝子情報が公開されてからわずか9カ月足らずで、NIHなどとともに臨床試験を完了させたのです(図表1)。
臨床試験の段階においてはトランプ前政権が打ち出した新型コロナウイルス・ワクチンの開発・製造・流通を加速させる政策「ワープ・スピード作戦」が作用したということもありますが、驚くべきスピードであることに間違いはありません。
モデルナの『2020年アニュアルレポート』などによると、同社の新型コロナウイルス・ワクチンは、米国の他にも、EU、日本、カナダ、韓国、フィリピン、英国、スイス、コロンビア、イスラエル、台湾、カタール、シンガポールへの供給について契約を締結したとされています。日本では、モデルナのワクチンは、ファイザー製とアストラゼネカ製に加えて、2021年5月21日に厚生労働省によって特例承認されています。